Bosutinib in der Erstlinientherapie der Chronischen Myeloischen Leukämie
Die frühe Nutzenbewertung von Bosutinib (Bosulif®) ist das dritte Verfahren zu neuen Arzneimitteln bei der chronischen myeloischen Leukämie (CML), das zweite Verfahren zu Bosutinib. In diesem Verfahren geht es um die Zulassung von Bosutinib zur Behandlung von Erwachsenen mit neu diagnostizierter Philadelphia-Chromosom-positiver chronischer myeloischer Leukämie (Ph+ CML) in der chronischen Phase (CP). Der G-BA hat Imatinib, Nilotinib oder Dasatinib als zweckmäßige Vergleichstherapie festgelegt und das IQWiG mit der Dossierbewertung beauftragt. Pharmazeutischer Unternehmer und IQWiG kommen zu unterschiedlichen Bewertungen. Einen Überblick über Bewertungsvorschläge von pharmazeutischem Unternehmer und IQWiG sind in Tabelle 1 zusammengefasst.
Tabelle 1: Vorschläge zum Zusatznutzen von Bosutinib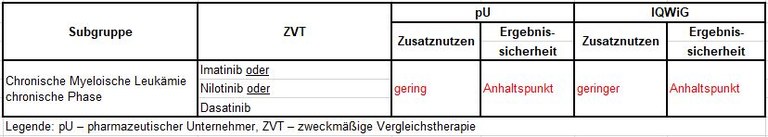
Unsere Anmerkungen sind:
- Bosutinib ist ein Tyrosinkinase-Inhibitor (TKI) der zweiten Generation. Er ist der vierte zugelassene TKI für die Erstlinientherapie von CML-Patienten in der chronischen Phase.
- Basis der frühen Nutzenbewertung ist BFORE, eine offene randomisierte Studie zum Vergleich von Bosutinib (400 mg/Tag) versus Imatinib (400 mg/Tag).
- Bosutinib führt zu einer höheren Rate guter molekularer Remissionen, nicht zu einer Erhöhung der ereignisfreien und der Gesamtüberlebensrate. Die Gesamtüberlebensrate liegt in beiden Studienarmen nach 2 Jahren bei >96%.
- Tiefe molekulare Remissionen sind Voraussetzung für ein kontrolliertes Absetzen des TKI und für ein langes rezidivfreies Überleben. Das Erreichen einer guten molekularen Remission ist ein patientenrelevanter Endpunkt.
- Schwere unerwünschte Nebenwirkungen traten unter Bosutinib insgesamt häufiger als unter Imatinib auf, einzelne Nebenwirkungen waren seltener. Einige der Bosutinib-assoziierten Nebenwirkungen, wie z. B. die Diarrhoe, sind zeitlich begrenzt und selbstlimitiert.
- Eine frühere Studie (BELA) zum Vergleich von Bosutinib (500 mg) versus Imatinib (400 mg) war negativ in Bezug auf den primären Endpunkt der kompletten zytogenetischen Remission (CCyR).
- Der für Bosutinib gegenüber Imatinib gesehene Vorteil liegt im Bereich des Vorteils von Nilotinib (ENESTnd-Studie) und Dasatinib (Dasision-Studie) gegenüber Imatinib. Daten zum direkten Vergleich von Bosutinib mit anderen Zweitgenerations-TKI liegen nicht vor.
