Abemaciclib beim HR+, metastasiertem Mammakarzinom
Abemaciclib ist zugelassen in der Erst- und der Zweitlinientherapie des lokal fortgeschrittenen oder metastasierten, HR-positiven, HER2-negativen Mammakarzinoms in Kombination mit antihormoneller Therapie. Inhalt dieses Verfahrens ist die frühe Nutzenbewertung von Abemaciclib in Kombination mit Fulvestrant. Das IQWiG wurde mit dem Bericht beauftragt. Subgruppen, zweckmäßige Vergleichstherapie sowie Bewertungsvorschläge sind in Tabelle 1 zusammengefasst.
Tabelle 1: Berechnung des Zusatznutzens durch pU und IQWiG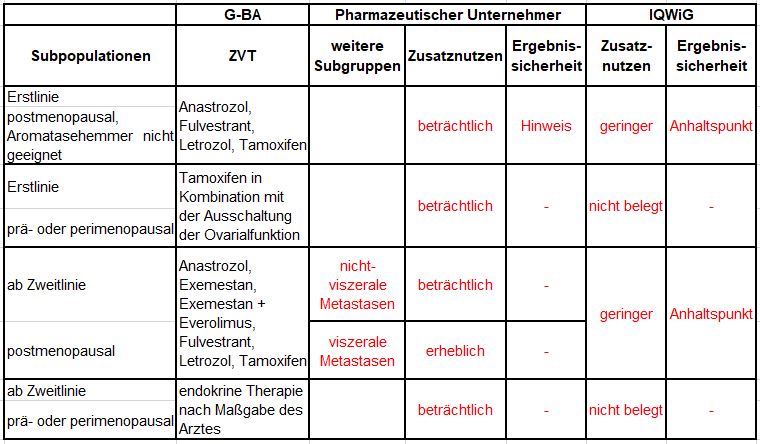
Unsere Anmerkungen sind:
- Basis der frühen Nutzenbewertung bei den postmenopausalen Patientinnen ist MONARCH-2, eine internationale, multizentrische, Placebo-kontrollierte Phase-III-Studie zum Vergleich von Abemaciclib + Fulvestrant vs Fulvestrant. Die zweckmäßige Vergleichstherapie entspricht den Empfehlungen der Fachgesellschaften in Bezug auf die endokrine Therapie, es fehlt allerdings der Hinweis auf die Empfehlungen zur inzwischen etablierten Kombination mit CDK4/6 Inhibitoren.
- Abemaciclib + Fulvestrant führt gegenüber Aromatasehemmer zur signifikanten Erhöhung der Remissionsrate und zur Verlängerung der progressionsfreien Überlebenszeit (Median 7,1 Monate; HR 0,55), nicht der Gesamtüberlebenszeit.
- Die Zeit bis zur Verschlechterung einiger belastender Symptome wie Appetitlosigkeit, Fatigue, finanziellen Schwierigkeiten, Schlaflosigkeit und Schmerz wird durch Abemaciblib verlängert.
- Die Rate schwerer, Therapie-assoziierter Nebenwirkungen ist im Abemaciclib- viel höher als im Kontroll-Arm. Die häufigste Nebenwirkung unter Abemaciclib ist Diarrhoe.
- In der Bewertung des klinischen Nutzens auf der ESMO-Magnitude of Clinical Benefit Scale v1.1 erhält Abemaciclib in Kombination mit Fulvestrant den Grad 3 (Skala 1 (niedrig) – 5 (hoch)).
Mit Palbociclib, Ribociclib und Abemaciclib sind inzwischen drei CDK4/6 Inhibitoren zur Kombination mit endokriner Therapie bei Patientinnen mit lokal fortgeschrittenem oder metastasiertem Mammakarzinom in der Erstlinientherapie zugelassen. Für die genauere Einordnung der drei Substanzen sind längere Verlaufsbeobachtungen und direkt vergleichende Studien erforderlich.
Abemaciclib Aromatasehemmer DGHO Stellungnahme 20190222
Abemaciclib Fulvestrant DGHO Stellungnahme 20190222
