Bosutinib in der Zweit- und Drittlinientherapie der chronischen myeloischen Leukämie (CML)
Die erneute Nutzenbewertung von Bosutinib (Bosulif®) bei vorbehandelten Patienten mit Philadelphia-Chromosom-positiver (Ph+), chronischer myeloischer Leukämie (CML) erfolgt nach Aufhebung des Orphan-Drug-Status. Bosutinib ist zugelassen zur Behandlung von Erwachsenen mit Ph+ CML in der chronischen Phase, der akzelerierten Phase und der Blastenkrise nach Vorbehandlung mit mindestens einem Tyrosinkinaseinhibitor und wenn Imatinib, Nilotinib und Dasatinib nicht als geeignete Behandlungsoption angesehen werden. Zwischenzeitlich wurde auch ein Verfahren zur Nutzenbewertung von Bosutinib in der Erstlinientherapie durchgeführt. Der G-BA hat Ponatinib oder Interferon alpha als zweckmäßige Vergleichstherapien in Abhängigkeit vom Krankheitsstadium festgelegt und das IQWiG mit der Dossierbewertung beauftragt. Pharmazeutischer Unternehmer und IQWiG kommen zu identischen Bewertungen. Einen Überblick über die Bewertungsvorschläge von pharmazeutischem Unternehmer und IQWiG sind in Tabelle 1 zusammengefasst.
Tabelle 1: Vorschläge zum Zusatznutzen von Bosutinib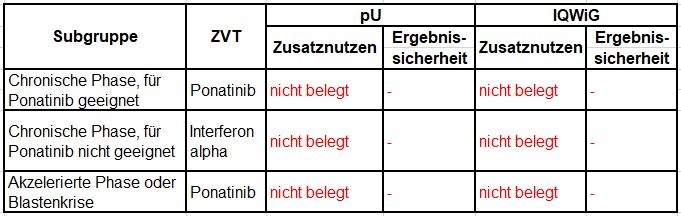
Legende: pU – pharmazeutischer Unternehmer, ZVT – zweckmäßige Vergleichstherapie
Unsere Anmerkungen sind:
- Bosutinib ist ein Tyrosinkinase-Inhibitor (TKI) der zweiten Generation. Nach Aufhebung des Orphan-Drug-Status wird Bosutinib neu bewertet bei Patienten nach Vorbehandlung mit mindestens einem Tyrosinkinaseinhibitor und wenn Imatinib, Nilotinib und Dasatinib nicht als geeignete Behandlungsoption angesehen werden.
- Wichtige Kriterien für die Therapieentscheidung bei diesen Patienten sind das Ansprechen auf die Vortherapie, das Vorliegen einer TKI-Resistenz, Komorbidität und das Nebenwirkungsrisiko. Zweckmäßige Vergleichstherapie ist eine patientenindividuelle Behandlung. Dies weicht von der Festlegung des G-BA mit Begrenzung auf Posatinib und Interferon alpha ab.
- Basis der frühen Nutzenbewertung sind 73 zulassungskonforme Patienten der nichtrandomisierten Zulassungsstudie 3160A4-200.
- Bosutinib führt zu zytogenetischen und molekularen Remissionen, die Ansprechraten sind unterschiedlich in Abhängigkeit vom Krankheitsstatus. Daten vergleichender Studien gegenüber anderen TKI liegen nicht vor.
Alle für die CML zugelassenen TKI haben ihr charakteristisches Nebenwirkungsprofil. Insbesondere für Patienten mit Vorliegen oder mit erhöhtem Risiko kardiovaskulärer Komplikationen ist Bosutinib eine wirksame, medikamentöse Alternative.
