Cemiplimab beim kutanen Plattenepithelkarzinom
Cemiplimab gehört zur Substanzklasse der PD-1-Inhibitoren. Es ist zugelassen zur Behandlung von erwachsenen Patienten mit metastasiertem oder lokal fortgeschrittenem kutanen PEK, die für eine kurative Operation oder kurative Strahlentherapie nicht in Betracht kommen. Der G-BA hat zwei Subgruppen gebildet und das IQWiG mit der Dossierbewertung beauftragt. Der pharmazeutischer Unternehmer schlägt eine weitere Subgruppenbldung für Patienten nach vorheriger medikamentöser Therapie vor. Pharmazeutischer Unternehmer und IQWiG kommen zu unterschiedlichen Bewertungen. Einen Überblick über Vergleichstherapie und Bewertungsvorschläge gibt Tabelle 1.
Tabelle 1: Vorschläge zum Zusatznutzen von Cemiplimab beim kutanen Plattenepithelkarzinom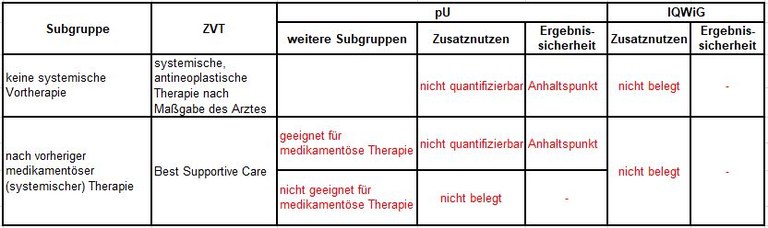
Unsere Anmerkungen sind:
- Beim fortgeschrittenen oder metastasierten, kutanen Plattenepithelkarzinom gibt es einen ungedeckten medizinischen Bedarf. Die Tumoren befinden sich zu einem Großteil in der Kopf-Hals-Region und führen im Rezidiv nach operativer/strahlentherapeutischer Vorbehandlung zu ausgeprägten Entstellungen wie auch funktionellen Problemen. Auch in der metastasierten Situation gibt es für diese Indikation keine zugelassenen Arzneimittel und keine systemische Standardtherapie.
- Zweckmäßige Vergleichstherapie bei geeigneten Patienten ist eine systemische Therapie nach Maßgabe des behandelnden Arztes, bei nicht geeigneten Patienten Best Supportive Care.
- Basis der frühen Nutzenbewertung ist R2810-ONC-1540, eine multinationale, nicht-randomisierte Studie. Aus dieser Studie wurde die Daten der Patientengruppe 3 mit der zugelassenen Dosierung von Cemiplimab ausgewertet.
- Unter Cemiplimab erreichten 40% der Patienten eine Remission, die Remissionen sind nachhaltig.
- Cemiplimab ist gut verträglich. Das Nebenwirkungsprofil entspricht den PD-1-Inhibitoren.
Mit Cemiplimab hat sich das Behandlungsportfolio für diese klinisch problematische Patientengruppe sinnvoll erweitert. Cemiplimab ist wirksam, der Therapieeffekt ist nachhaltig. Eine Quantifizierung des Zusatznutzens ist mangels vergleichender Daten nicht möglich.
