Olaparib beim BRCAmut Mammakarzinom
27.11.2019
Die frühe Nutzenbewertung von Olaparib (Lynparza®) ist das erste Verfahren zu einem PARP-Inhibitor in der Therapie des fortgeschrittenen oder metastasierten Mammakarzinoms. Die Zulassung ist beschränkt auf Patienten* mit HER2 negativem, BRCA mutiertem Mammakarzinom nach Vortherapie mit einem Anthrazyklin und einem Taxan in der (neo-)adjuvanten oder metastasierten Situation.
Das IQWiG wurde mit dem Bericht beauftragt. Subgruppen, zweckmäßige Vergleichstherapie sowie die unterschiedlichen Bewertungsvorschläge sind in Tabelle 1 zusammengefasst.
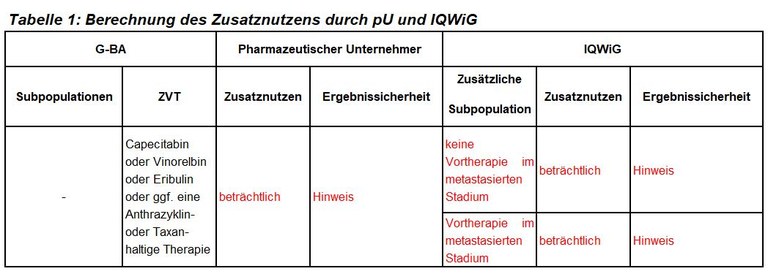
Unsere Anmerkungen sind:
- Die zweckmäßige Vergleichstherapie entspricht weitgehend den Empfehlungen der Fachgesellschaften. Die zunehmend häufig eingesetzten Platinderivate sind eine chemotherapeutische Alternative, formal jedoch in dieser Indikation nicht zugelassen.
- Basis der frühen Nutzenbewertung zum Vergleich von Olaparib vs Chemotherapie (nach Wahl des behandelnden Arztes) beim BRCA-mutierten, fortgeschrittenen/metastasierten Mammakarzinom nach Chemotherapie mit Anthrazyklin und Taxanen ist OlympiAD.
- Olaparib führt zu einer Steigerung der Remissionsrate, zur Verlängerung des progressionsfreien Überlebens und zur Reduktion belastender Nebenwirkungen. Die Überlebenszeit wurde in der Gesamtstudienpopulation nicht verlängert.
- In der Bewertung des klinischen Nutzens auf der ESMO-Magnitude of Clinical Benefit Scale v1.1 erhält Olaparib den Grad 4 (Skala 1 (niedrig) – 5 (hoch)).
Olaparib ist eine wertvolle Bereicherung der Therapieoptionen in einer molekularbiologisch definierten Subgruppe des metastasierten Mammakarzinoms mit großem, ungedecktem medizinischem Bedarf.
