Ropeginterferon alfa-2b bei Polycythaemia vera
Dies ist das zweite Verfahren im Rahmen der frühen Nutzenbewertung für ein neues Arzneimittel zur Therapie der Polycythaemia vera. Ropeginterferon alfa-2b (Besremi®) ist zugelassen für Patienten mit Polycythemia vera ohne klinische Zeichen einer Splenomegalie. Ropeginterferon alfa-2b hat in diesem Verfahren keinen Orphan-Drug-Status. Das IQWiG wurde mit dem Bericht beauftragt. Subgruppen, zweckmäßige Vergleichstherapie sowie Bewertungsvorschläge sind in Tabelle 1 zusammengefasst.
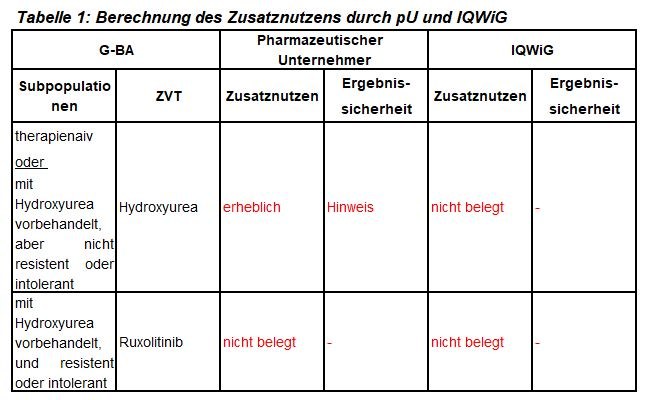
Unsere Anmerkungen sind:
- Die zweckmäßige Vergleichstherapie entspricht weitgehend unseren Empfehlungen. Die EU-Zulassung geht über die Einschlusskriterien der Zulassungsstudie hinaus.
- Basis der Zulassung ist PROUD-PV, eine internationale, multizentrische, randomisierte, offene Studie zum Vergleich von Ropeginterferon alfa-2b versus Hydroxyurea mit 257 Patienten. Basis des Dossiers des pharmazeutischen Unternehmers ist CONTINUATION-PV, eine Extensionsstudie mit einer Verlaufsbeobachtung von inzwischen 4 Jahren mit 171 Patienten. Die längere Beobachtungszeit ist sinnvoll angesichts der langsamen Wirkung von Ropeginterferon alfa-2b.
- Ropeginterferon alfa-2b führt gegenüber Hydroxyurea zu einer höheren hämatologischen Ansprechrate und zu einer höheren Rate molekularer Remissionen nach 36 und 48 Monaten. Die Rate molekularer Remission Ropeginterferon alfa-2b steigt im Verlauf der Beobachtungsstudie kontinuierlich an.
- Die Rate thrombembolischer Ereignisse ist in beiden Studienarmen niedrig. Die Rate sekundärer Malignome ist höher im Hydroxyurea-Arm. Bei den Auswertungen zur Gesamtüberlebenszeit, zur Lebensqualität, zur Rate schwerer Nebenwirkungen und zur Abbruchrate zeigen sich keine Unterschiede in den beiden Studienarmen.
- Das Dossier des pharmazeutischen Unternehmers ist unvollständig und enthält nicht alle Daten, die zwischenzeitlich auf internationalen Kongress präsentiert worden sind. Insbesondere fehlen Daten zur Gesamtpopulation der Zulassungsstudie PROUD-PV sowie eine vollständige Darstellung der unerwünschten Ereignisse.
Interferon alpha ist eine wichtige Alternative in der Therapie von Patienten mit behandlungsbedürftiger Polycythaemia vera. Interferon alpha wurde von uns schon in den vergangenen Jahren als gleichwertige Therapie der Polycythaemia vera empfohlen, u. a. bei jüngeren Patienten (vor allem Frauen) mit Kinderwunsch, bei schwangeren Patientinnen mit Hoch- und Intermediärrisiko-Profil oder bei Patienten mit Intoleranz auf Aderlass. Die Zulassung von Ropeginterferon alfa-2b füllt sowohl in der Primär- als auch Zweit- oder Mehrlinientherapie der PV eine bereits seit mehreren Jahrzehnten bestehende Lücke. Die Nachbeobachtungszeit ist für eine nachhaltige Nutzenbewertung zu kurz.
