Cabozantinib beim medullären Schilddrüsenkarzinom
09.11.2021
Die erneute Nutzenbewertung von Cabozantinib (Cometriq®) wird nach Ablauf der im ersten Verfahren festgelegten Frist durchgeführt.
Cabozantinib ist zugelassen für die Therapie des medullären Schilddrüsenkarzinoms (MTC) bei erwachsenen Patient*innen mit progredienter, nicht resektabler, lokal fortgeschrittener oder metastasierter Erkrankung. Cabozantinib hat den Status eines Medikamentes für seltene Leiden (Orphan Drug). Der Bericht wurde vom G-BA erstellt. Einen Überblick über Vergleichstherapie und Bewertungsvorschläge gibt Tabelle 1.
Tabelle 1: Berechnung des Zusatznutzens durch pU und IQWiG
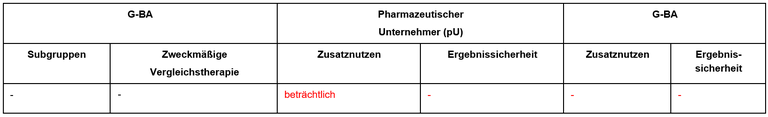
Unsere Anmerkungen sind:
- Im Unterschied zu Vandetanib (Erstlinientherapie) und Selpercatinib (Zweitlinientherapie) hat Cabozantinib einen Orphan-Drug-Status in dieser Indikation. Deshalb wurde vom G-BA keine Zweckmäßige Vergleichstherapie (ZVT) festgelegt. Standard bei Therapie-fähigen und -bedürftigen Patient*innen ist die Therapie mit einem Multikinase-Inhibitor, also hier der Vergleich mit Vandetanib. Ein indirekter Vergleich der Zulassungsstudien der beiden TKI ist allerdings aufgrund relevanter Unterschiede im Studiendesign nicht möglich.
- Basis der frühen Nutzenbewertung von Cabozantinib ist EXAM, eine multizentrische, randomisierte, Placebo-kontrollierte Phase-III-Studie mit einer Cabozantinib-Dosierung von 140 mg. Die Datenlage hat sich seit der letzten Bewertung nicht substanziell geändert.
- Cabozantinib führte zu einer statistisch signifikanten und klinisch relevanten Verlängerung des progressionsfreien Überlebens (HR 0,28) und zu einer Reduktion krankheitsassoziierter Symptome.
- In der Gesamtpopulation der Patient*innen führte Cabozantinib nicht zu einer Verlängerung der Überlebenszeit. Crossover war in der Studie nicht zugelassen, allerdings ist die Postprogressionstherapie nicht sorgfältig dokumentiert.
- In den Subgruppen der Patient*innen mit der RET-Mutation M918T führte Cabozantinib zur Verlängerung der Überlebenszeit. Die Zulassungsstudie war allerdings nicht dazu angelegt, Unterschiede in diesen Subgruppen nachzuweisen.
- Nebenwirkungen sind unter Cabozantinib häufig und führen bei der Mehrzahl der Patient*innen zu Dosisreduktionen.
- Im Dossier werden zusätzlich die Daten von EXAMINER, einer randomisierten Studie zum Nachweis der Nicht-Unterlegenheit einer Dosis von 60 mg in Tablettenform im Vergleich zu 140 mg als Kapsel präsentiert. Hier zeigt sich formal keine Unterlegenheit der niedrigeren Dosierung, nummerisch sind die Ergebnisse etwas ungünstiger.
- In der Bewertung des klinischen Nutzens auf der ESMO-Magnitude of Clinical Benefit Scale v1.1 erhält Cabozantinib den Grad 3 (Skala 1 (niedrig) – 5 (hoch)).
Cabozantinib ist einer von zwei wirksamen, oralen Tyrosinkinase-Inhibitoren (TKI) zur Erstlinientherapie von Patient*innen mit lokal fortgeschrittenem oder metastasiertem, progredientem, medullärem Schilddrüsenkarzinom.
