Nivolumab beim Adenokarzinom des oberen GI Traktes
Nivolumab ist zugelassen in Kombination mit fluoropyrimidin- und platinbasierter Kombinationschemotherapie für die Erstlinienbehandlung des HER2-negativen fortgeschrittenen oder metastasierten Adenokarzinoms von Ösophagus, gastroösophagealem Übergang oder Magen. Die Zulassung ist beschränkt auf Patient*innen mit einer höheren PD-L1-Expression (Combined Positive Score [CPS] ≥ 5) und ohne Nachweis einer Überexpression von HER2. Der G-BA hat mehrere Subgruppen gebildet. Das IQWiG wurde vom G-BA mit dem Bericht beauftragt. Pharmazeutisches Unternehmen und IQWiG kommen zu unterschiedlichen Bewertungen. Einen Überblick über Subgruppenbildung und Bewertungsvorschläge gibt Tabelle 1.
Tabelle 1: Berechnung des Zusatznutzens durch pU und IQWiG
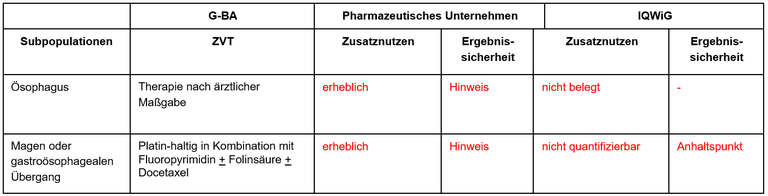
Unsere Anmerkungen sind:
- Die Subgruppenbildung ist nicht sinnvoll. In der Praxis werden die Adenokarzinome des oberen Gastrointestinaltrakts (Ösophagus, gastroösophagealer Übergang und Magen) im Stadium IV zu einer Behandlungsgruppe zusammen. Unterschieden wird nicht nach der Lokalisation, sondern nach biologischen Parametern wie HER2- und PD-L1-Expression.
- Die Kombination eines Platinderivats mit einem Fluoropyrimidin war Bestandteil des bisherigen Chemotherapie-Standards bei HER2-negativen Adenokarzinomen von Ösophagus, gastroösophagealem Übergang und Magen. Die Kombination ist als ZVT geeignet.
- Basis der frühen Nutzenbewertung zum Vergleich von Chemotherapie + Nivolumab vs Chemotherapie ist die internationale, multizentrische, offene Studie CheckMate 649.
- In der Gesamtstudie führte Nivolumab + Chemotherapie gegenüber Chemotherapie zu einer signifikanten Steigerung des progressionsfreien Überlebens und der Gesamtüberlebenszeit, u.a. ausgedrückt durch eine Verbesserung der Überlebensrate nach 3 Jahren. Der positive Einfluss auf die Gesamtüberlebenszeit in der Gesamtstudie ist vor allem auf Patient*innen mit einer höheren PD-L1-Expression (CPS ≥5) zurückzuführen.
- Die Nebenwirkungen entsprechen der Substanzklasse der Immuncheckpoint-Inhibitoren.
- In der Bewertung des klinischen Nutzens auf der ESMO-Magnitude of Clinical Benefit Scale v1.1 erhält Nivolumab den Grad 4 (Skala 1 (niedrig) – 5 (hoch)).
- Die Darstellung der PD-L1-Positivität im Dossier des pharmazeutischen Unternehmers ist etwas verwirrend: In den Legenden der Überlebenskurven scheint Positivität als CPS ≥1 definiert.
Die Daten der Studie CheckMate 649 etablieren die Immunchemotherapie als Standard in der Erstlinie von Patient*innen mit metastasiertem, HER2- negativem und PD-L1 exprimierendem Adenokarzinom von Ösophagus, gastroösophagealem Übergang und Magen mit einem PD-L1 CPS ≥5.
