Remdesivir bei COVID-19 und Risiko für einen schweren Verlauf der Infektion
Remdesivir ist zugelassen zur Behandlung von Erwachsenen, die keine zusätzliche Sauerstoffzufuhr benötigen und ein erhöhtes Risiko für einen schweren COVID-19-Verlauf haben. Der G-BA hat das IQWiG mit dem Bericht beauftragt. Pharmazeutischer Unternehmer und IQWiG kommen zu unterschiedlichen Bewertungen. Einen Überblick über Vergleichstherapie und Bewertungsvorschläge gibt Tabelle 1.
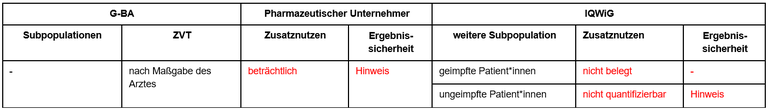
Tabelle 1: Berechnung des Zusatznutzens durch pU und IQWiG
Unsere Anmerkungen sind:
- Die Behandlung von COVID-19 hat sich in den letzten Monaten auf die Verhinderung schwerer Verläufe bei vulnerablen Patient*innen konzentriert.
- Die Festlegung der ZVT entspricht den aktuellen Empfehlungen. Inzwischen stehen mehrere, wirksame Arzneimittel in dieser Indikation zur Verfügung.
- Basis der frühen Nutzenbewertung von Remdesivir ist die internationale, Placebo-kontrollierte Phase-III-Studie GS-9012 (PINETREE). Aufgenommen wurden Patient*innen mit unterschiedlichen Risikofaktoren für einen schweren Verlauf
- Remdesivir führte zu einer Senkung der Hospitalisierungsrate. Todesfälle traten nicht auf.
- Unklar ist, ob und in welchem Maße
- die Wirksamkeit von Remdesivir bei Erkrankten vom Status der Immunabwehr (Schutzimpfung, genesen) beeinflusst wird,
- bestimmte Risikopatient*innen in stärkerem Maße von Remdesivir profitieren,
- die klinische Wirksamkeit bei den verschiedenen SARS-CoV-2-Varianten identisch ist.
- Die Verträglichkeit von Remdesivir ist gut, die Rate schwerer unerwünschten Ereignisse war niedriger als im Placebo-Arm.
In der Hämatologie und Onkologie wird der Einsatz von Remdesivir bei Patient*innen mit erhöhtem Risiko für einen schweren Verlauf mit dem Empfehlungsgrad B (niedrigster Grad E - höchster Grad A) empfohlen. Im Einzelfall ist eine Entscheidung zwischen Remdesivir, oralen Virostatika und Antikörpern erforderlich.
